Page 56 - Acalán 121
P. 56
Acalán 121 54 Julio - Diciembre
Proceso UV/H2O2 13.54 ppm). La baja ef ciencia de la reacción pudo
verse afectada por la recombinación de radicales
En este proceso se empleó el H2O2 como fuente •OH causada por una alta concentración de ellos
principal de •OH al irradiarse con luz UV. La f gura (Kim et al., 2013). Lester et al., (2011) observó en su
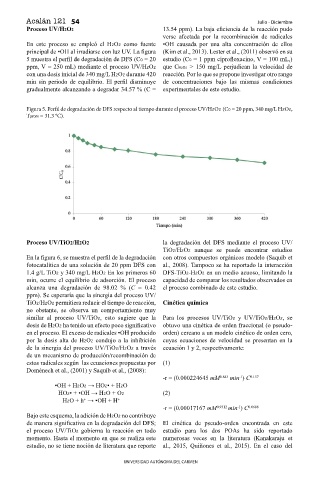
5 muestra el perf l de degradación de DFS (C0 = 20 estudio (C0 = 1 ppm ciprof oxacino, V = 100 mL,)
ppm, V = 250 mL) mediante el proceso UV/H2O2 que CH2O2 > 150 mg/L perjudican la velocidad de
con una dosis inicial de 340 mg/L H2O2 durante 420 reacción. Por lo que se propone investigar otro rango
min sin periodo de equilibrio. El perf l disminuye de concentraciones bajo las mismas condiciones
gradualmente alcanzando a degradar 34.57 % (C = experimentales de este estudio.
Figura 5. Per!l de degradación de DFS respecto al tiempo durante el proceso UV/H2O2 (C0 = 20 ppm, 340 mg/L H2O2,
Tprom = 31.3 °C).
Proceso UV/TiO2/H2O2 la degradación del DFS mediante el proceso UV/
TiO2/H2O2 aunque se puede encontrar estudios
En la f gura 6, se muestra el perf l de la degradación con otros compuestos orgánicos modelo (Saquib et
fotocatalítica de una solución de 20 ppm DFS con al., 2008). Tampoco se ha reportado la interacción
1.4 g/L TiO2 y 340 mg/L H2O2 En los primeros 60 DFS-TiO2-H2O2 en un medio acuoso, limitando la
min, ocurre el equilibrio de adsorción. El proceso capacidad de comparar los resultados observados en
alcanza una degradación de 98.02 % (C = 0.42 el proceso combinado de este estudio.
ppm). Se esperaría que la sinergia del proceso UV/
TiO2/H2O2 permitiera reducir el tiempo de reacción, Cinética química
no obstante, se observa un comportamiento muy
similar al proceso UV/TiO2, esto sugiere que la Para los procesos UV/TiO2 y UV/TiO2/H2O2, se
dosis de H2O2 ha tenido un efecto poco signif cativo obtuvo una cinética de orden fraccional (o pseudo-
en el proceso. El exceso de radicales •OH producido orden) cercano a un modelo cinético de orden cero,
por la dosis alta de H2O2 condujo a la inhibición cuyas ecuaciones de velocidad se presentan en la
de la sinergia del proceso UV/TiO2/H2O2 a través ecuación 1 y 2, respectivamente:
de un mecanismo de producción/recombinación de
estos radicales según las ecuaciones propuestas por (1)
Domènech et al., (2001) y Saquib et al., (2008):
-1
-r = (0.000224645 mM 0.843 min ) C 0.157
•OH + H2O2 → HO2• + H2O
HO2• + •OH → H2O + O2 (2)
+
H2O + h → •OH + H +
-r = (0.00017167 mM 0.9312 min ) C 0.0688
-1
Bajo este esquema, la adición de H2O2 no contribuye
de manera signif cativa en la degradación del DFS; El cinética de pseudo-orden encontrada en este
el proceso UV/TiO2 gobierna la reacción en todo estudio para los dos POAs ha sido reportado
momento. Hasta el momento en que se realiza este numerosas veces en la literatura (Kanakaraju et
estudio, no se tiene noción de literatura que reporte al., 2015, Quiñones et al., 2015). En el caso del
UNIVERSIDAD AUTÓNOMA DEL CARMEN