Page 77 - Acalán 121
P. 77
Julio - Diciembre Acalán 121 75
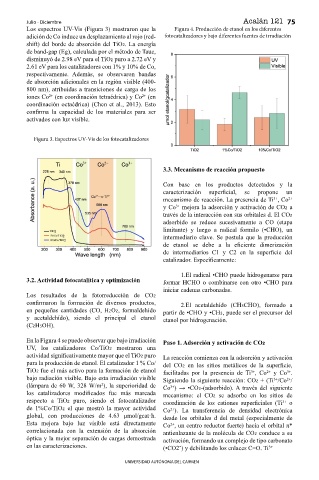
Los espectros UV-Vis (Figura 3) mostraron que la Figura 4. Producción de etanol en los diferentes
adición de Co induce un desplazamiento al rojo (red- fotocatalizadores y bajo diferentes fuentes de irradiación
shift) del borde de absorción del TiO2. La energía
de band-gap (Eg), calculada por el método de Tauc,
disminuyó de 2.98 eV para el TiO2 puro a 2.72 eV y
2.61 eV para los catalizadores con 1% y 10% de Co,
respectivamente. Además, se observaron bandas
de absorción adicionales en la región visible (400-
800 nm), atribuidas a transiciones de carga de los
2+
2+
iones Co (en coordinación tetraédrica) y Co (en
coordinación octaédrica) (Chen et al., 2013). Esto
conf rma la capacidad de los materiales para ser
activados con luz visible.
Figura 3. Espectros UV-Vis de los fotocatalizadores
3.3. Mecanismo de reacción propuesto
Con base en los productos detectados y la
caracterización superf cial, se propone un
mecanismo de reacción. La presencia de Ti , Co
3+
2+
y Co mejora la adsorción y activación de CO2 a
3+
través de la interacción con sus orbitales d. El CO2
adsorbido se reduce sucesivamente a CO (etapa
limitante) y luego a radical formilo (•CHO), un
intermediario clave. Se postula que la producción
de etanol se debe a la ef ciente dimerización
de intermediarios C1 y C2 en la superf cie del
catalizador. Específ camente:
1. El radical •CHO puede hidrogenarse para
3.2. Actividad fotocatalítica y optimización formar HCHO o combinarse con otro •CHO para
iniciar cadenas carbonadas.
Los resultados de la fotorreducción de CO2
conf rmaron la formación de diversos productos, 2. El acetaldehído (CH3CHO), formado a
en pequeñas cantidades (CO, H2O2, formaldehído partir de •CHO y •CH3, puede ser el precursor del
y acetaldehído), siendo el principal el etanol etanol por hidrogenación.
(C2H5OH).
En la Figura 4 se puede observar que bajo irradiación Paso 1. Adsorción y activación de CO22
UV, los catalizadores Co/TiO2 mostraron una
actividad signif cativamente mayor que el TiO2 puro La reacción comienza con la adsorción y activación
para la producción de etanol. El catalizador 1 % Co/ del CO2 en los sitios metálicos de la superf cie,
TiO2 fue el más activo para la formación de etanol facilitadas por la presencia de Ti , Co y Co .
2+
3+
3+
bajo radiación visible. Bajo esta irradiación visible Siguiendo la siguiente reacción: CO2 + (Ti /Co /
3+
2+
(lámpara de 60 W, 328 W/m²), la superioridad de Co ) → •CO2-(adsorbido). A través del siguiente
3+
los catalizadores modif cados fue más marcada mecanismo: el CO2 se adsorbe en los sitios de
respecto a TiO2 puro, siendo el fotocatalizador coordinación de los cationes superf ciales (Ti o
3+
de 1%Co/TiO2 el que mostró la mayor actividad Co ). La transferencia de densidad electrónica
2+
global, con producciones de 4.63 μmol/gcat·h. desde los orbitales d del metal (especialmente de
Esta mejora bajo luz visible está directamente Co , un centro reductor fuerte) hacia el orbital π*
2+
correlacionada con la extensión de la absorción antienlazante de la molécula de CO2 conduce a su
óptica y la mejor separación de cargas demostrada activación, formando un complejo de tipo carbonato
en las caracterizaciones. (•CO2 ) y debilitando los enlaces C=O. Ti 3+
-
UNIVERSIDAD AUTÓNOMA DEL CARMEN